【写在前面】
本期推荐的是由南昌大学附属医院等研究团队合作近期发表于PeerJ 的一篇文章,揭示USP22可作为骨肉瘤糖酵解途径的关键调节因子。下面就先跟着小森一起来解读一下吧~
1. 本研究通过整合多种生物信息学工具并结合临床数据,系统、全面地探索了USP22在骨肉瘤发生、进展和预后中的功能,确定潜在机制。
2. 本研究通过多数据库挖掘治疗靶点,从GEO 数据库中获得与骨肉瘤相关的转录组学数据集,进而结合TCGA数据集、STRING数据库、DAVID数据库获得了344个共表达基因,提高了数据来源的广泛性。
3. 在利用生物信息学分析数据的基础上,结合体外实验,进一步验证USP22对骨肉瘤细胞生长的影响及其机制。“干湿结合”增强实验结果的可靠性。
总的来说,这篇文章研究了骨肉瘤糖酵解途径的关键调节因子USP22的致癌作用,通过整合生物信息学分析和体外实验分析并验证了USP22的下调可以抑制骨肉瘤细胞的糖酵解和生长,完整性高,逻辑思维也比较强!对于这个思路,小伙伴们有没有兴趣应用在自己的研究中呢?想要了解生信数据挖掘,或是对数据库和生信工具使用感到迷茫的老铁们,快来和小森聊聊,小森一定帮你有的放矢!
【题目及作者信息】

【摘要】(阅读原文为主)
骨肉瘤是最常见的原发性恶性骨肿瘤,但发病机制尚不清楚。研究表明,泛素特异性加工肽酶22(USP22)高表达,与癌症中的肿瘤恶性肿瘤和预后相关。作者团队整合了GEO和TCGA数据库的转录组学数据集和骨肉瘤的临床信息,通过差异表达分析、加权基因共表达网络分析以及富集分析,探讨了USP22共表达基因的生物学功能和信号通路。并体外实验证实了生物信息学分析的准确性和可靠性。结果表明,USP22在骨肉瘤的发生、发展和预后中起着关键作用。说明了USP22的下调可以抑制骨肉瘤细胞的糖酵解和生长。
【方法】
整合GEO和TCGA数据库的转录组学数据集和骨肉瘤的临床信息,以评估USP22在骨肉瘤中的表达和预后价值。进行差异表达分析和加权基因共表达网络分析(WGCNA)鉴定USP22相关共表达基因。通过基因本体论(GO)和京都基因与基因组百科全书(KEGG)富集分析,探讨USP22共表达基因的生物学功能和信号通路。为验证生物信息学分析的准确性,使用 siRNA 下调骨肉瘤细胞系 Sao-2中USP22 的表达,并评估其对细胞增殖、迁移、侵袭、凋亡和关键信号通路调控的影响。
【结果部分】
USP22在骨肉瘤中高表达,与预后不良相关
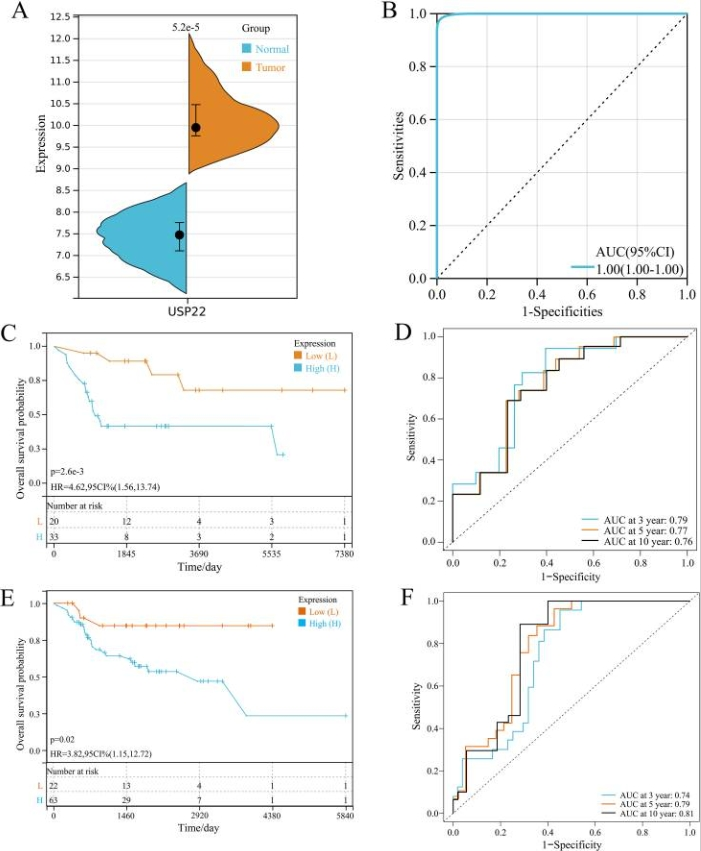
图1 USP22在骨肉瘤中的表达及预后分析。
USP22共表达基因的鉴定
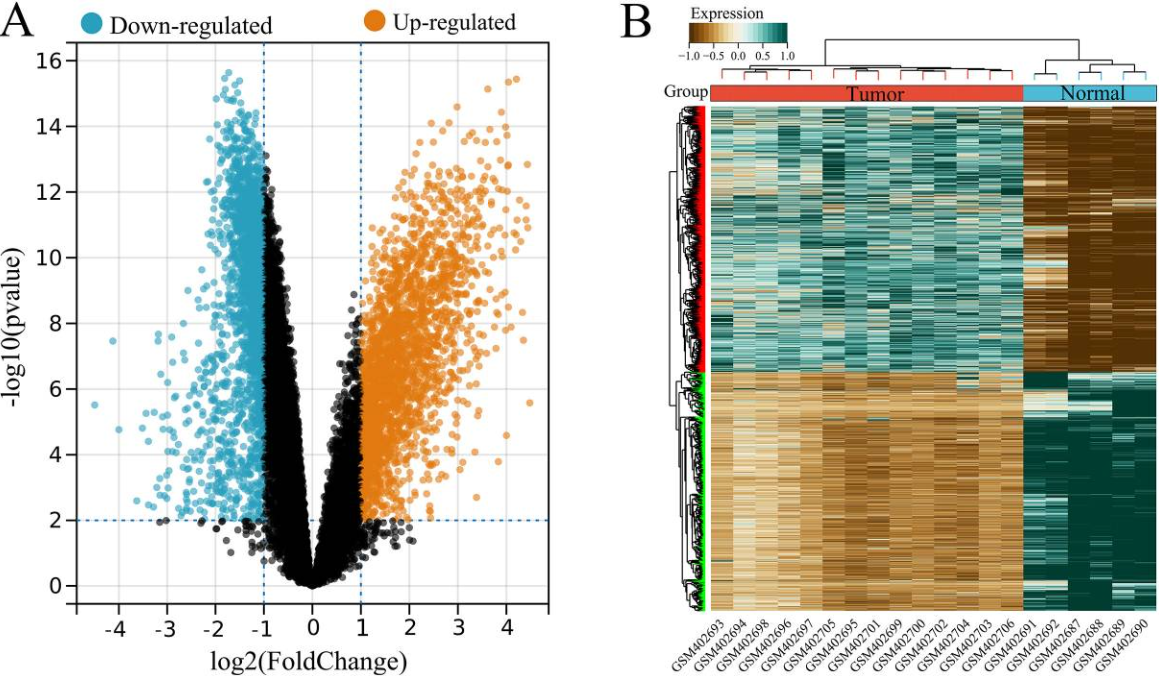
图2 GSE16088数据集中USP22相关差异表达基因 (DEGs) 的鉴定。
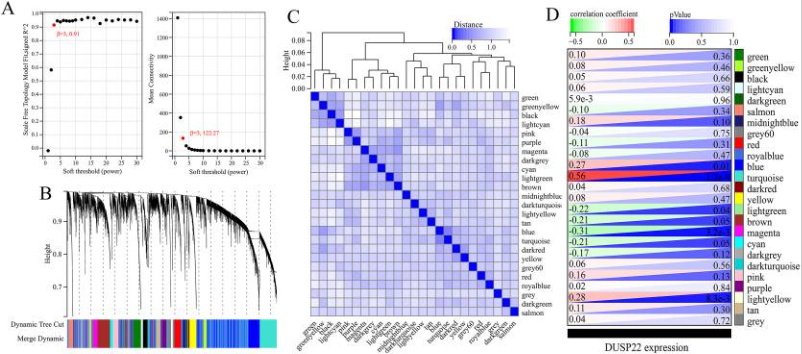
图3 使用加权基因共表达网络分析(WGCNA) 鉴定TCGA-OS数据集中USP22相关的共表达基因。
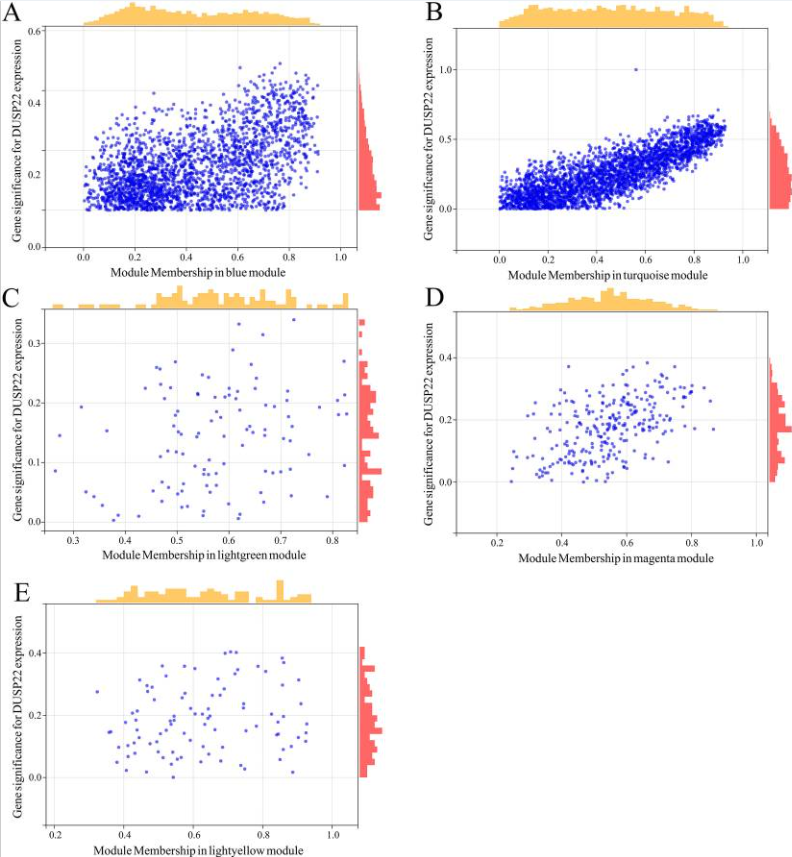
图4 鉴定与USP22共表达的关键基因。
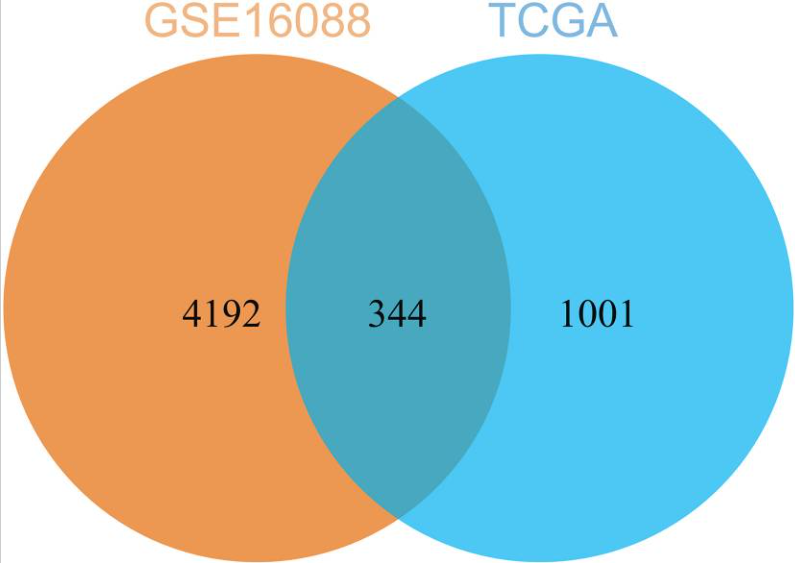
图5通过比较TCGA-OS队列的DEG和数据集中的hub gens GSE16088确定的常见基因。
PPI网络分析与功能富集分析
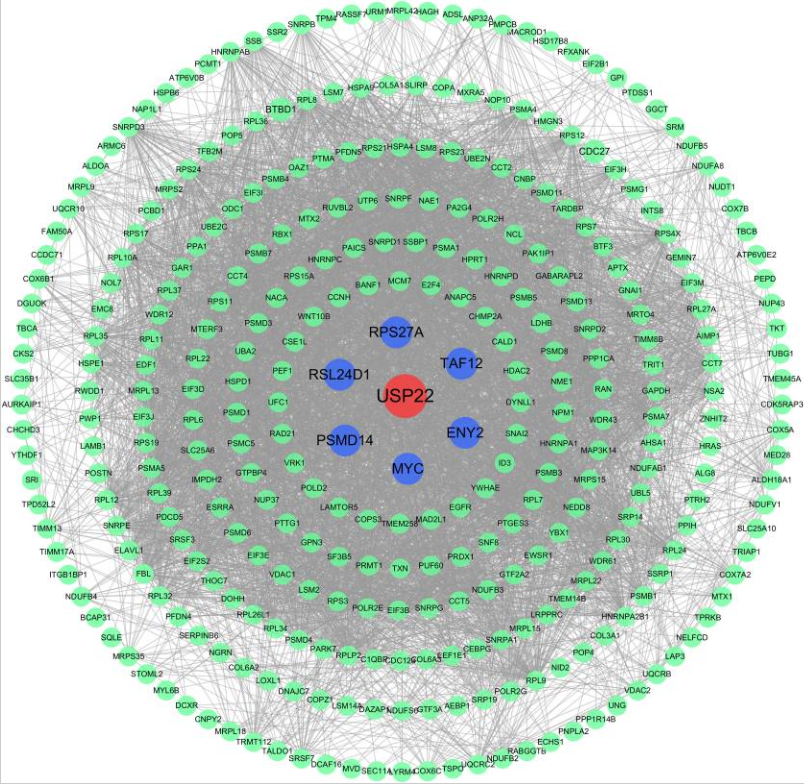
图6 蛋白质-蛋白质相互作用 (PPI) 网络分析。
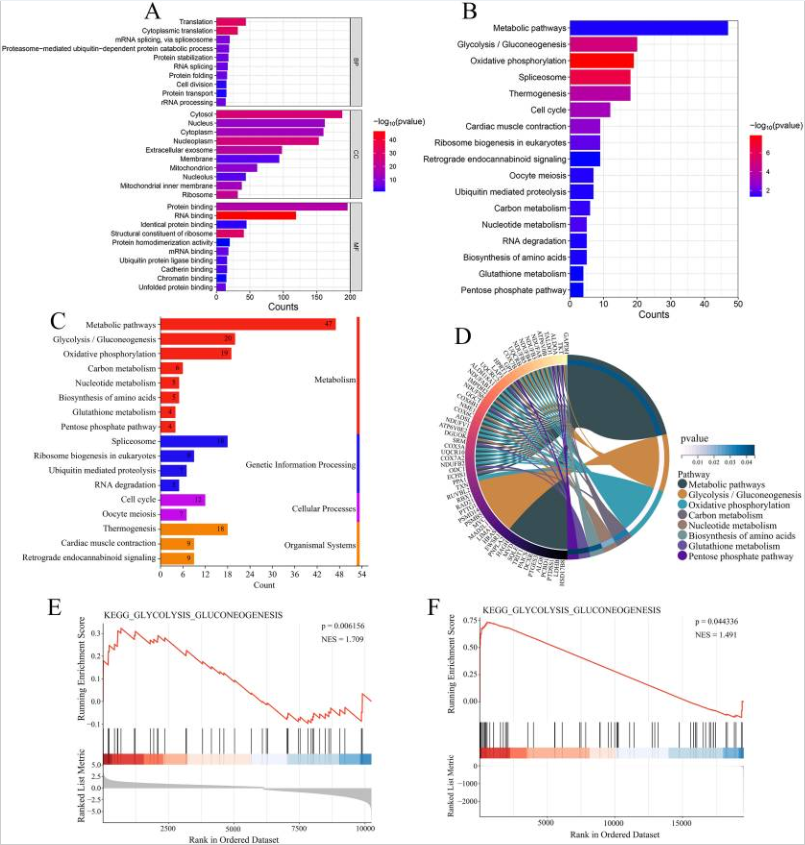
图7 344个共表达基因的功能富集分析。
USP22下调抑制Sao-2增殖

图8 USP22敲低对骨肉瘤细胞增殖的影响。
USP22下调抑制Sao-2细胞的迁移和侵袭
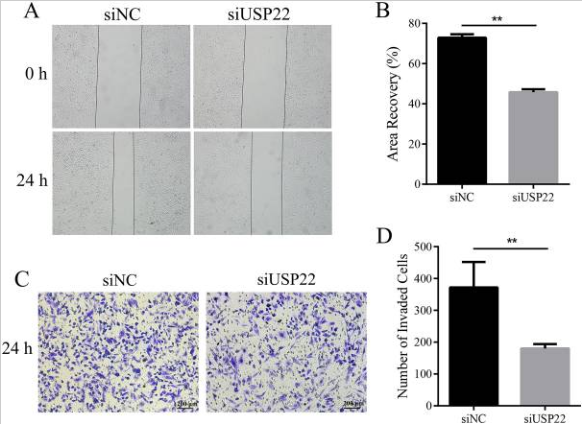
图9 USP22下调对骨肉瘤细胞迁移和侵袭的影响。
USP22下调诱导Sao-2细胞凋亡

图10 USP22下调对骨肉瘤细胞凋亡的影响。
USP22的下调抑制Sao-2细胞中的需氧糖酵解水平
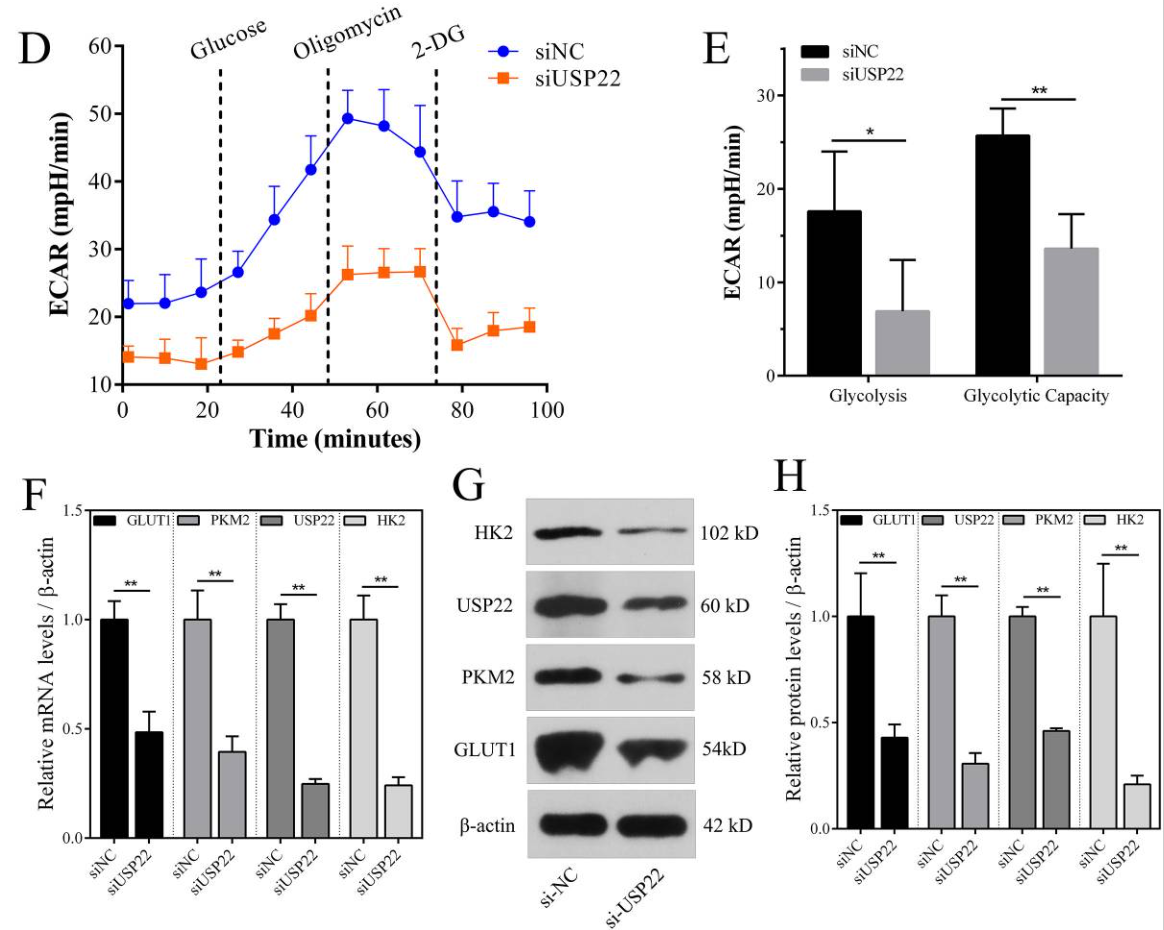
图11 USP22 敲低对骨肉瘤细胞中有氧糖酵解水平的影响。
【结论与讨论】
作者团队研究证明了USP22在骨肉瘤中的致癌作用。根据生物信息学分析,USP22在骨肉瘤中高度表达,并与患者的生存率低有关。USP22促进骨肉瘤的分子机制涉及多种信号通路,包括糖酵解、氧化磷酸化、剪接体、产热和细胞周期。体外实验进一步验证了生物信息学分析结果的准确性。研究表明,USP22的下调可以抑制骨肉瘤细胞的糖酵解和生长。
原文链接:www.ncbi.nlm.nih.gov/pmc/articles/PMC11114114/